Résumé
Pour transmettre l’information nerveuse, les neurones utilisent différents signaux chimiques parmi lesquels figurent plus d’une centaine de peptides différents. La plupart de ces peptides déclenchent des comportements spécifiques et cohérents et sont liés à bon nombre de désordres neurologiques. Il est de plus en plus admis que dans le traitement de l’information, les signaux peptidiques jouent un rôle très différent de celui des neurotransmetteurs classiques.
Neurotransmetteurs versus neuropeptides
Les neuropeptides constituent une importante et vaste classe de messagers moléculaires transportant l’information entre les neurones du cerveau. Il existe plus de 100 neuropeptides différents dans le cerveau de mammifère, et la plupart d’entre eux sont fabriqués et libérés à partir de l’hypothalamus. Certains neuropeptides hypothalamiques sont libérés directement dans la circulation sanguine, et exercent leurs effets périphériques tout comme des hormones. Parmi ces neurones hypothalamiques, les neurones magnocellulaires à ocytocine et vasopressine se sont avérés être un système modèle, car révélateur d’aspects majeurs de nombreuses fonctions neuronales, incluant les mécanismes de libération des neuropeptides eux-mêmes. Le système classique de communication inter neuronale s’effectue via des neurotransmetteurs, molécules conditionnées dans de petites vésicules libérées principalement au niveau de la synapse neuronale. Par contre, les neuropeptides, contenus dans d’autres vésicules, sont libérés via des mécanismes différents de ceux des neurotransmetteurs classiques, à partir de nombreux sites membranaires incluant les terminaisons nerveuses, les corps cellulaires et les dendrites des neurones. Les mécanismes de libération des neuropeptides au niveau des dendrites peuvent être tout à fait différents de ceux mis en jeu au niveau des terminaisons axonales et, pour la vasopressine et l’ocytocine, cette régulation différentielle permet aux effets périphériques du neuropeptide libéré de se réaliser de façon indépendante de ses effets centraux.
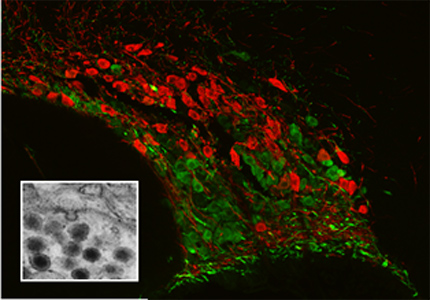
Figure 1: Dans le noyau supraoptique, les dendrites des neurones à vasopressine (en vert) et ocytocine (en rouge) projettent vers la surface ventrale du cerveau. Encart : le profil membranaire en forme d’oméga (fusion de la vésicule à la membrane), capturé dans une section de microscopie électronique, correspond au creux de la membrane dendritique restant après libération d’une vésicule.
Message secret versus message publique
Les neuropeptides interagissent habituellement avec des récepteurs couplés aux protéines G, pour activer des voies de signalisation pouvant affecter différentes fonctions cellulaires. Les neuropeptides agissent souvent de façon rétrograde sur leurs cellules d’origine, par exemple pour faciliter le développement d’un patron particulier d’activité électrique. Leur action peut s’étendre également aux cellules voisines pour engager collectivement l’activité d’une population neuronale en un signal cohérent et unique. Finalement, le signal de sortie de la population ainsi coordonnée peut induire à son tour des pulses de sécrétion peptidique pouvant agir dans le cerveau, selon un signal analogue à des pulses d’hormone. A ces sites distants de leur lieu de sécrétion, les neuropeptides peuvent reprogrammer les réseaux neuronaux, via leurs effets sur l’expression des gènes, la synaptogénèse, et au travers des nouvelles connections câblées fonctionnelles, amorcer une libération activité-dépendante. Les neurotransmetteurs classiques font passer des “secrets chuchotés” d’une cellule particulière à une autre; ils transmettent un message qui a de l’importance à un temps donné et à un site particulier. Par contre, les neuropeptides sont des “annonceurs publics”, leurs messages perdurent, au moins quelques temps; et se transmettent non d’une cellule à l’autre, mais d’une population de neurones à une autre population – tels des signaux hormonaux.
———————-
“…. les traits comportementaux s’accompagnent d’altérations de la distribution de l’expression des récepteurs des neuropeptides.”
———————-
Premier objectif: l’amorçage
Dans l’hypothalamus, de larges quantités d’ocytocine et de vasopressine sont libérées par les dendrites neuronales, indépendamment de la libération par les terminaisons nerveuses. Cette libération dendritique peut être modulée par un phénomène “d’amorçage” qui implique la fabrication préalable de nombreuses vésicules, disponibles pour une libération activité-dépendante subséquente de neuropeptide. Cet “amorçage” accroît ainsi la capacité qu’ont les interactions locales à coordonner l’activité neuronale. En favorisant l’intercommunication, les peptides peuvent ainsi “reprogrammer” le comportement d’un système neuronal. Ils peuvent également “préparer” les régions cibles du cerveau qui possèdent leurs récepteurs, déclenchant une cascade d’évènements permettant une réorganisation fonctionnelle des réseaux neuronaux, temporaire, mais fournissant le substrat pour des effets comportementaux prolongés.
Puis les effets comportementaux
De nombreux peptides ont des effets comportementaux spécifiques. Par exemple, l’ocytocine est impliquée dans les comportements sociaux, incluant le lien social et le comportement maternel; et la vasopressine agit dans le cerveau pour affecter la reconnaissance sociale et l’agression. D’autres peptides libérés par d’autres cellules nerveuses ont des effets sur d’autres comportements et émotions. Par exemple, le neuropeptide Y augmente la prise alimentaire et les orexines régulent le sommeil et l’état de veille par des interactions avec les systèmes neuronaux étroitement liés aux émotions, la récompense, et l’homéostasie énergétique. Ce sont les expériences de manipulation génétique, comme les mutations transgéniques ou les transferts de gènes viraux, qui ont mis en évidence la nature hormonale des effets comportementaux des peptides, et montré que les traits comportementaux s’accompagnent d’altérations de la distribution et de l’expression des récepteurs des neuropeptides.

Figure 2: “Le cerveau Wifi”. La libération peptidique non synaptique par les neurones magnocellulaires de l’hypothalamus peut “rediffuser”, à la façon des hormones, un signal qui déclenche les comportements peptides-dépendants.
Actuellement, les études translationnelles commencent à extrapoler à la recherche humaine, les concepts émergeant des études de cognition sociale et de comportement social chez l’animal. La vasopressine et l’ocytocine ont été liées à des troubles neurologiques humains tels le trouble d’anxiété sociale, la dépression, la schizophrénie et les troubles du spectre autistique (TSA). De plus, les troubles de la régulation de l’appétit, de la libido et de l’humeur font partie des nombreux objectifs potentiels des thérapies basées sur l’utilisation des peptides. Dans le futur, “sniffer” des analogues neuropeptidiques (par administration intra nasale), peut constituer un moyen pour les neuropeptides d’accéder directement au cerveau, et leur diffusion vers leurs sites récepteurs peut être une voie alternative pour le traitement de plusieurs de ces troubles.
Document à télécharger : PDF
Traduction :
Françoise Moos, Institut CNRS de Neurosciences cellulaire et intégrative,Université de Strasbourg, France
Cette brève est produite par la British Society for Neuroendocrinology et peut être utilisée librement pour l’enseignement de la neuroendocrinologie et la communication vers le public.
©British Society for Neuroendocrinology et Société de Neuroendocrinologie pour la traduction.
