Résumé
La fréquence de l’obésité et des pathologies qui y sont associées telles que diabète, hypertension et dyslipidémie (constituant le ” syndrome métabolique “) atteint des proportions épidémiques dans les pays industrialisés. Nous proposons ici une hypothèse selon laquelle l’horloge biologique, qui nous prépare normalement chaque matin à être actif la journée, est altérée par notre style de vie moderne de faible activité pendant la journée et d’ingestion d’aliments jusqu’en fin de soirée. De plus nous passons en revue les données anatomiques en accord avec notre proposition, selon laquelle un déséquilibre du système nerveux autonome pourrait conduire à la survenue simultanée du diabète de type 2, d’une hypertension, d’une dyslipidémie et d’une obésité viscérale.
L’horloge biologique qui rythme notre vie
Les causes des mécanismes à l’origine du syndrome métabolique sont encore mal connues. Pour expliquer l’envolée de l’obésité, un consensus général s’accorde à impliquer, d’une part, l’abondance de nourriture dans les sociétés modernes et, d’autre part, le fait que l’évolution nous a façonné pour des périodes de disette plutôt que d’abondance. De surcroît, nos systèmes homéostatiques façonnés par l’évolution ont ” appris ” à s’adapter au cycle perpétuel de lumière et d’obscurité, de sorte que notre corps anticipe la survenue du sommeil et de la période active. Dans tous les organismes, des mécanismes se sont développés pour prédire quand le jour commence ou s’arrête ; ces mécanismes constituent le ” système circadien “. Dans toutes les cellules du corps, des horloges ont évolué dans un sens ou dans un autre pour assurer un contrôle temporel. Cependant, dans le cerveau, et plus précisément à la base de l’hypothalamus ventral, se situe la seule horloge biologique autonome, les noyaux suprachiasmatiques (SCN). En distribuant un message temporel via des hormones et le système nerveux autonome, les SCN transmettent leur signal journalier à tous les tissus de l’organisme. A l’aide de ces signaux, les mécanismes homéostasiques des tissus sont préparés aux périodes d’activité ou de repos. Cet héritage supplémentaire de l’évolution a été développé pour nous permettre de prédire les changements environnementaux favorables à la veille ou au sommeil. L’avantage d’une telle prédiction est de permettre à notre corps d’anticiper ces changements et d’accumuler ou de libérer les métabolites en vue de leur utilisation ultérieure comme substrat énergétique nécessaire au labeur de la journée.
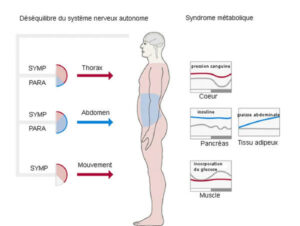
Le mode de vie peut provoquer des perturbations des sorties de l’horloge biologique en modifiant l’équilibre sélectif du système nerveux autonome dans différentes régions du corps. Dans le compartiment intra-abdominal, la sortie du système nerveux autonome est orientée vers la branche parasympathique, ce qui provoque une forte sécrétion d’insuline, une croissance du tissu adipeux intra-abdominal, et un foie plus gras. Au contraire, dans les compartiments du thorax et des membres, la branche sympathique prévaut, ce qui conduit à une forte pression artérielle et à une altération du transport du glucose du sang vers le muscle. Dans ce modèle, les symptômes du syndrome métabolique sont la conséquence, et non la cause, de la maladie.
Une ” mutation environnementale ” ?
Au cours du siècle dernier, les modes de vie ont énormément changé dans les pays industrialisés. La nourriture est devenue abondante. L’on observe également une augmentation du grignotage ainsi qu’un décalage du dernier repas en fin de soirée. Parallèlement, la nécessité de l’effort physique a considérablement diminué. De plus, l’activité physique n’a plus besoin de coïncider avec la phase d’éclairement (naturel). Dans de telles conditions, nous émettons l’hypothèse selon laquelle le cerveau perd son ” sens ” du rythme interne et externe. Par conséquent, l’environnement est perçu par le cerveau comme étant arythmique et aplati sur le plan métabolique. Dans une perspective d’évolution à long terme, ce changement peut être interprété comme une ” mutation ” subite de l’environnement. Etant donné que le cerveau utilise le système nerveux autonome pour distribuer la rythmicité interne, nous suggérons que le déséquilibre et l’arythmie du système nerveux autonome sont des causes majeures du syndrome métabolique.
——————–
…le cerveau perd son ” sens ” du rythme interne et externe.
——————–
L’équilibre de la vie
Le bien-fondé de cette proposition repose sur l’organisation des sorties du SCN via le système nerveux autonome. Bien que les SCN, via des sorties hypothalamiques, traduisent leur rythme à l’ensemble du corps à l’aide d’hormones hypophysaires, nous commençons seulement à évaluer la contribution du système nerveux autonome. L’avantage évident du système nerveux autonome est la bien meilleure résolution spatiale qu’il peut avoir pour distribuer les messages des SCN.
Pendant longtemps, le tissu adipeux a été considéré comme une structure-cible pour les hormones et seulement pour la branche sympathique du système nerveux autonome. Nous avons récemment démontré que les projections parasympathiques à partir du noyau moteur du nerf vague vers le tissu adipeux modulaient clairement la sensibilité de ce dernier à l’insuline ainsi que le métabolisme glucidique et lipidique d’une manière anabolique. Ceci permet au cerveau de stimuler, soit l’utilisation des graisses (voie sympathique), soit leur stockage (voie parasympathique). Nous avons également montré au sein du cerveau qu’il existait une surprenante capacité des neurones des SCN à se spécialiser. Par exemple, des neurones ” pré-autonomes ” présents dans les SCN ainsi que dans d’autres régions hypothalamiques émettent des projections spécifiques vers la région intra-abdominale ou vers le compartiment sous-cutané. Cela signifie que les organes intra-abdominaux, comme le tissu adipeux viscéral, le foie, ou le pancréas, reçoivent des afférences des mêmes neurones (hypothalamiques). Etant donné que la prise alimentaire stimule la sortie parasympathique vers le pancréas et provoque une sécrétion d’insuline, la conséquence de ce câblage du système nerveux autonome est que le même stimulus va augmenter la sensibilité à l’insuline du foie et celle de la graisse viscérale. Comme les repas du soir sont connus pour provoquer une augmentation de la sécrétion d’insuline, une pénétration plus efficace du glucose dans le tissu adipeux sera accompagnée d’une accumulation plus facile des graisses.
Pour résumer, nous voyons, en raison du changement de style de vie des pays industrialisés, que le syndrome métabolique est en phase ascendante, pas nécessairement à cause d’une prise alimentaire exagérée, mais en raison d’horaires de repas au mauvais moment.
Traduction :
Etienne Challet, CNRS UMR7168 – Université Louis Pasteur Strasbourg
Cette brève est produite par la British Society for Neuroendocrinology et peut être utilisée librement pour l’enseignement de la neuroendocrinologie et la communication vers le public.
©British Society for Neuroendocrinology et Société de Neuroendocrinologie pour la traduction.
