Résumé
Le cannabis agit en mimant les endocannabinoïdes qui sont des modulateurs naturels spécifiques des récepteurs CB1 dans le cerveau et les tissus périphériques. Ces molécules augmentent l’appétit par une double action, à la fois sur l’envie et le plaisir du repas. De plus, elles favorisent le stockage de l’énergie dérivée des aliments sous forme de graisse qui se dépose dans le tissu adipeux. Ces découvertes ont laissé suggérer que des bloquants des récepteurs CB1 pourraient être utilisés en tant que médicaments anti-obésité.
Le pouvoir de la nourriture
En biologie, on considère généralement la prise alimentaire comme un des éléments du système homéostasique chargé d’équilibrer l’apport et la dépense énergétique afin de maintenir la stabilité du poids corporel. Bien que de tels modèles soient utiles et leur efficacité avérée dans d’autres domaines de la physiologie (par exemple la régulation fine de l’équilibre hydrique, la régulation de la soif et de l’ingestion de sodium), notre appétit pour la nourriture est par ailleurs soumis à de puissantes influences d’ordre psychologique. La plupart d’entre nous résistent mal en présence d’un buffet bien rempli, certains allant même jusqu’à surmonter un malaise d’ordre physique afin de s’empiffrer d’un dessert appétissant. La goinfrerie fait partie de notre héritage évolutif et, loin de maintenir un équilibre strict entre apport et dépense énergétique, nos mécanismes motivationnels s’efforcent au contraire d’augmenter la prise de nutriments et l’activité de systèmes particulièrement efficaces pour un stockage presque illimité de l’énergie excédentaire. Notre susceptibilité aux propriétés sensorielles, ou même seulement à l’idée de celles-ci, est une des causes principales de l’obésité : la conséquence de systèmes psychologiques qui répondent à la variété et au goût agréable de la nourriture dans un monde de tentations où abondent les hamburgers et autres gateaux à la crème, sans compter les sodas renforcés en sucre, les charcuteries et le chocolat !
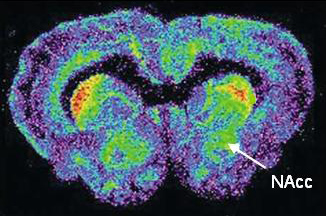
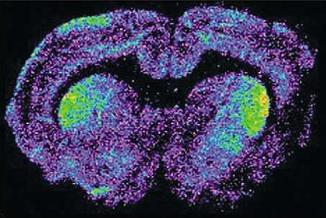
| Images en pseudocouleurs illustrant la densité des récepteurs CB1 dans le cerveau de rat au niveau du noyau accumbens (NAcc). Comparé à un animal contrôle recevant un régime standard (panneau du haut), un animal devenu obèse par surconsommation d’une nourriture hautement palatable et riche (régime cafétéria) (panneau du bas) montre une diminution marquée de la densité des récepteurs CB1 au niveau du Nacc. Ce changement est attribué à une “down-régulation” des récepteurs CB1 suite à une augmentation de la libération des endocannabinoïdes en réponse aux propriétés sensorielles du régime cafétéria, de sa surconsommation et du développement de l’obésité. |
Modèles avaricieux et hédonistes
Des données récentes ont renforcé l’idée qu’il existe deux systèmes en interaction pour le contrôle central de l’appétit, le premier régulant le “besoin” et l’autre le “plaisir” de manger. Le système dopaminergique méso-limbique qui prend son origine dans l’aire tegmentale ventrale et se termine dans le noyau accumbens est la clé du “besoin” de manger et il évalue la valeur incitative ou la force motivationnelle de la nourriture. Il nous oriente vers des stimuli liés à la nourriture qui, quand nous sommes affamés, accentuent notre intérêt pour des nouvelles sources de nutriments. Par ailleurs, des circuits neuronaux au sein du noyau accumbens sont l’autre clé qui permet l’évaluation hédoniste de la nourriture au moment même où nous l’ingérons, influençant ainsi la taille du repas et encourageant une surconsommation de nourritures palatables (agréables au goût). La manipulation pharmacologique des activités de ces deux systèmes peut influencer de manière critique la façon dont nous voudrons ou aimerons la nourriture, déterminant ainsi, si et quelle quantité en sera ingérée.
Les cannabinoïdes dans le besoin et le plaisir
Les actions psychoactives de la marijuana (Cannabis sativa) dépendent de l’action agoniste du delta9-tetrahydrocannabinol (THC) sur les récepteurs CB1 exprimés dans différentes régions cérébrales, incluant les systèmes “besoin” et “plaisir” centrés sur le noyau accumbens. Les “grignotages” (munchies) du folklore du cannabis dérivent de la capacité du THC à mimer l’action des agonistes naturels (endogènes) de ces récepteurs : les endocannabinoïdes. Des milliers d’années d’expérience de la “fumette” ont permis de commencer à comprendre le rôle biologique de ces neuromodulateurs dans le contrôle physiologique de l’appétit par le cerveau.
———————-
… L’obésité a été liée à des niveaux élevés d’activité cannabinoïde dans le cerveau et à la périphérie…
———————-
L’administration intracérébrale (particulièrement au niveau du noyau accumbens) des endocannabinoïdes anandamide, 2-arachidonoylglycerol (2-AG) ou ether de noladine stimule la prise de nourriture chez les animaux de laboratoires alors qu’un blocage avec des antagonistes des récepteurs CB1, comme le rimonabant, la diminue. Les études comportementales montrent que le cannabinoïdes augmentent principalement la valeur incitative de la nourriture : même des rats complètement rassasiés se remettent à manger (et même s’il doivent travailler durement pour ce faire!). Le jeûne qui augmente naturellement l’envie de manger est associé à une augmentation des niveaux centraux d’anandamide et de 2-AG. ; ce qui potentialise l’activité du réseau ” besoin ” mésolimbique.
Les endocannabinoïdes semblent aussi capable de moduler les aspects hédoniques des repas : le “plaisir” des repas après stimulation des récepteurs CB1 est souvent rapporté par les fumeurs de cannabis. Les animaux de laboratoires ne peuvent nous donner des évaluations subjectives mais des paradigmes comportementaux appropriés révèlent que l’anandamide, le 2AG et le THC produisent tous les trois des changements de comportement compatibles avec une plus grande palatabilité de la nourriture (alors que les antagonistes CB1 ont l’effet inverse) ; ceci est d’autant plus vrai lorsque l’anandamide est injecté directement dans le noyau accumbens.
Une cible thérapeutique toujours d’actualité
Les endocannabinoïdes ont également été impliqués dans les mécanismes métaboliques périphériques qui sous-tendent le stockage de l’énergie excédentaire dans le tissu adipeux. Le foie et les cellules adipeuses expriment des récepteurs CB1 et leur stimulation par des agonistes amènent à une accélération de la lipogénèse. Un effet inverse est observé avec les antagonistes CB1 qui pourraient peut-être augmenter la dépense énergétique. L’obésité a été liée à des niveaux élevés d’activité cannabinoïde dans le cerveau comme en périphérie.
L’action combinée des antagonistes CB1 sur les systèmes centraux et périphériques a mené presque naturellement à leur promotion comme agents anti-obésité, le rimonabant étant le premier agent de cette classe à pouvoir être prescrit afin de diminuer le poids corporel et normaliser le syndrome métabolique lié à l’obésité. Jusqu’à présent, l’usage de tels médicaments a été ralenti par des effets secondaires qui reflètent l’implication des endocannabinoïdes dans de nombreuses fonctions physiologique et psychologiques.
Quoiqu’il en soit, le système endocannabinoïde, avec son double aspect motivationnel et métabolique, représente toujours une cible pharmacologique fascinante pour le traitement des troubles de l’appétit ou du poids corporel et les maladies associées.
Traduction et adaptation :
Jacques Epelbaum, INSERM U894, Paris
Cette brève est produite par la British Society for Neuroendocrinology et peut être utilisée librement pour l’enseignement de la neuroendocrinologie et la communication vers le public.
©British Society for Neuroendocrinology et Société de Neuroendocrinologie pour la traduction.